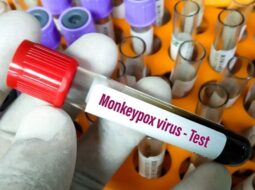
Sono sufficienti sessanta minuti dal momento dell'infusione delle Car-T - terapie cellulari avanzate che utilizzano le cellule del proprio sistema immunitario per combattere i tumori ematologici - per capire se il paziente rischia di sviluppare neurotossicità nei giorni successivi.
Il rivoluzionario studio dei ricercatori dell'Irccs Policlinico di Sant'Orsola di Bologna
Una novità resa possibile da strutture biologiche grandi appena 100 nanometri: le vescicole extracellulari. È quanto emerge da uno studio scientifico dell'Irccs Policlinico di Sant'Orsola di Bologna, pubblicato sul Journal of clinical investigation.
I ricercatori della Piattaforma Ibt (Immunobiologia dei trapianti e delle terapie cellulari) hanno scoperto un metodo per prevedere con diversi giorni d'anticipo la probabile insorgenza dell'Icans, ovvero la sindrome da neurotossicità associata a terapia con cellule immunoeffettrici, un effetto collaterale che interessa circa un terzo dei pazienti oncoematologici trattati con le Car-T e che si manifesta a 5-7 giorni di distanza dall'infusione sotto forma di confusione, disturbo del linguaggio, disturbo motorio e convulsioni. Nei casi più gravi può portare al coma o al decesso.
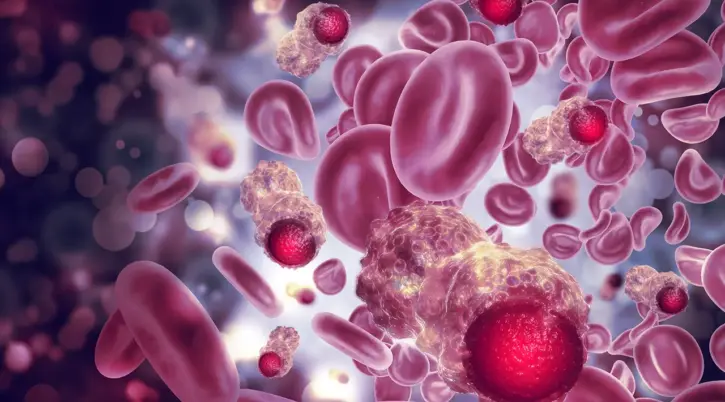
La Car-T per riconoscere e abbattere le cellule tumorali
L’immunoterapia ha rivoluzionato il trattamento di alcuni tumori, prima incurabili, ed è diventata uno dei pilastri dell’innovazione per la terapia del cancro.
Si basa sul concettorivoluzionario di combattere i tumori come se fossero un’infezione, ovvero “armando” il sistema immunitario del paziente in maniera tale da riconoscere le cellule tumorali eannientarle. Tra i vari trattamenti di immunoterapia oncologica la terapia con ChimericAntigen Receptors (CAR) T-cell ha dimostrato in modo consistente la sua efficacia sui tumori ematologici. Le CAR-T rappresentano la medicina personalizzata nel campo dei tumori. Ogni dose viene sviluppata e prodotta per un singolo paziente partendo dalle suestesse cellule immunitarie. Le prime approvazioni in Italia per l’applicazione delle CAR-T riguardano tumori del sangue quali linfomi nell’adulto e leucemia linfoblastica nel bambino.Una nuova CAR-T è in fase di approvazione anche per il mieloma multiplo. Alcuni studi sonoin corso, inoltre, per testare l’efficacia delle CAR-T nelle malattie autoimmuni neurologiche(disturbi dello spettro della neuromielite ottica [NMOSD], sclerosi multipla, miasteniagravis, etc).
Questi presidi innovativi hanno un rischio di neurotossicità acuta (ICANS) a carico del SNC,riportata nel 40-70% dei casi. L’ICANS si manifesta prevalentemente con un quadro di encefalopatia frontale, caratterizzato da un’iniziale comparsa di difficoltà di attenzione, riflessi arcaici, disturbi della scrittura e dell’eloquio, con possibile evoluzione verso una afasia globale/mutismo acinetico, sopore, crisi epilettiche/stato epilettico convulsivo o nonconvulsivo (questi ultimi riportati fino al 10% dei casi). In rari casi, 1-2%, può presentarsi unquadro di edema cerebrale fulminante che spesso è fatale.
Sebbene la patogenesi dell’ICANS sia ancora incerta, la sindrome da rilascio di citochine(CRS) che precede in genere l’ICANS, ed è scatenata dall’infusione di CAR-T, potrebbe giocare un ruolo significativo nell’indurre la neurotossicità.
Tuttavia, molte sono ancora le aree grigie da chiarire: la presenza di condizioni pre-disponenti, il meccanismo fisiopatologico correlato alla comparsa di manifestazioni neurologiche focali nonostante la frequente negatività del neuroimaging, le possibili strategie di prevenzione o mitigazione del danno neurologico, l’effetto a lungo termine delleCAR-T specialmente sugli aspetti cognitivi, l’incidenza di eventuali quadri di neurotossicitàtardiva, infine il “best treatment” (“escalation” o “aggressive therapy”?) della neurotossicità acuta, salvaguardando l’outcome ematologico.
I vantaggi: terapia ad hoc e degenza più breve
La ricerca dimostra che un'alta concentrazione di vescicole extracellulari nel sangue, misurata a un'ora di distanza dall'infusione della terapia cellulare, si correla fortemente allo sviluppo della sindrome entro la settimana successiva. Conoscere in anticipo il probabile sviluppo di questa complicanza consente non solo di modulare per tempo la risposta terapeutica, ma anche di accorciare i tempi di degenza. Al momento, infatti, i pazienti restano ricoverati per circa due settimane a scopo precauzionale: grazie a questa novità, i casi ritenuti non a rischio potranno invece essere dimessi in sicurezza.
Un risultato eccezionale
"Si tratta di un risultato eccezionale, un ulteriore passo in avanti per una terapia che rappresenta una delle frontiere più innovative e promettenti nella lotta a mielomi e linfomi", commenta Francesca Bonifazi, direttrice della Piattaforma di Immunobiologia dei trapianti e delle terapie cellulari e dell'unità operativa complessa "Trapianto e Terapie Cellulari in Ematologia" dell'Irccs.
L'importanza degli esami diagnostici specializzati nella prevenzione dei tumori ematologici
Gli esami diagnostici specializzati nella prevenzione dei tumori ematologici sono fondamentali per identificare precocemente eventuali alterazioni nel sangue e nel midollo osseo, permettendo una diagnosi tempestiva e migliorando così le probabilità di successo nel trattamento. I tumori ematologici, come le leucemie, i linfomi e il mieloma multiplo, possono svilupparsi con rigonfiamenti di ghiandole, ma anche senza sintomi evidenti nelle fasi iniziali, quindi gli esami sono cruciali per una diagnosi precoce.
Ecco alcuni dei principali esami diagnostici utilizzati:
- Esame emocromocitometrico (emocromo): Un test di laboratorio che misura il numero e la qualità delle cellule del sangue (globuli rossi, globuli bianchi e piastrine). Alterazioni nei valori possono suggerire la presenza di tumori ematologici.
- Citofluorometria (flow cytometry): Viene utilizzata per analizzare le cellule del sangue e identificare cellule anomale o maligne, come quelle presenti in leucemie o linfomi.
- Biopsia del midollo osseo: Un esame invasivo che consente di prelevare un campione di midollo osseo per identificare eventuali anomalie, come la proliferazione di cellule tumorali. È particolarmente utile per diagnosticare leucemie e mieloma multiplo.
- Elettroforesi delle proteine: Utilizzata per diagnosticare il mieloma multiplo, questo test separa le proteine nel sangue e può rilevare la presenza di proteine anomale prodotte dalle cellule tumorali.
- Risonanza magnetica (RM) e tomografia computerizzata (TC): Questi esami di imaging possono essere utilizzati per individuare eventuali masse o linfonodi ingrossati, comuni in linfomi e leucemie.
- Test genetici e molecolari: Permettono di identificare mutazioni genetiche o alterazioni cromosomiche che possono predisporre a malattie ematologiche come leucemie acute o linfomi. Questi test sono anche importanti per la personalizzazione del trattamento.
- Test per il marker CD19 e CD20: Utilizzati principalmente nei linfomi, per identificare specifiche proteine sulla superficie delle cellule tumorali.
- Test per la mutazione BCR-ABL: Fondamentale per diagnosticare la leucemia mieloide cronica, dove è presente una mutazione genetica specifica.